Fusion: Stellarator (Wendelstein 7-X), Tokamak (ITER) & Andere
01.11.2015 um 03:02Die Idee ist Kernfusion, aber dachte es sei keine schelchte Idee weiter auszuholen, deswegen vorab etwas Chemie und Kernspaltung.Gim schrieb:Ist die Überschrift vielleicht falsch gewählt? Du hast zwar mit Kernfusion begonnen, jetzt scheint dieser Thread aber zunehmend allgemein kernphysikalische Gebiete zu thematisieren. Vielleicht solltest du den Threadnamen ändern lassen, denn mit Kernfusion hat die Kernspaltung nur am Rande, Chemie praktisch gar nichts zu tun.
Ja hat es bis auf Ausnahmen gleich viele Elektronen. Ich wollt es einfach halten, aber war wohl schlecht formuliert.Gim schrieb:Was genau meinst du damit, wie kann ein Atom "zuwenig" Elektronen haben. Ein Atom hat schließlich immer soviele Elektronen in der Hülle wie Protonen im Kern. Was genau bewirkt, das eine Bindung favorisiert wird?
Ob und wie Elektronen an andere Elemnte abgegeben werden hängt von der Elektronegativität ab..muss ich jetzt weiter ausholen; Elektronen befinden sich nicht alle auf denselbem Oribtal um den Atomkern. "Valenzelektronen" sind die äussersten Elektronen, die sich in den äußersten Atomorbitalen aufhalten. Diese können sich an Atombindungen beteiligen. Das war mit Mangel/Überschuss gemeint.
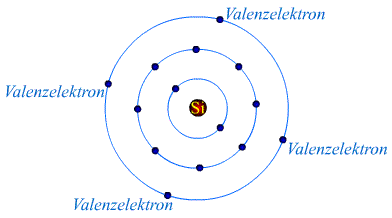
Umso kleiner der Radius und umso mehr Valenzelektronen ein Atom besitzt, umso besser kann es seine Elektronen "festhalten" und weitere anlagern. Man spricht dann von einem grossen "EN", was bedeutet, dass dies leichter Elektronen aufnehmen kann. Solche Elemente gehören zu den Nichtmetallen. Umso grösser der Atomradius eines Elements ist und umso weniger Valenzelektronen ein Element hat, desto eher verliert es seine Elektronen. Es hat eine kleine EN und die Tendenz, Elektronen abzugeben. Solche Elemente gehören zu den Metallen.
EN=Elektronegativität, ein Mass für das Vermögen eines Atoms, Bindungselektronen an sich zu ziehen.
Wer mehr darüber erfahren möchte, kann nach folgenden Stichworten googlen
-Edelgaskonfiguration und Oktettregel
-Elektronegativität
-Ionenbindung
Obiges Bsp mit Wasser und Sauerstoffatom fällt in die Kategorie "Atombindung", dann wenn zwei Atome mit einem hohen EN Wert sich Elektronen "teilen" und so eine "Atomare Bindung" eingehen.

ok danke, das hier ist PolyvinilchloridGim schrieb:Das ist nur die Summenformel des Monomers, Vinylchlorid. Die Summenformel eines Polymers zu nennen könnte sich als schwierig erweisen.
http://de.webqc.org/molecular-weight-of-%28C2H3Cl%29n.html
https://prezi.com/adqx3w3mwx9p/polyvinyl-chloride-c2h3cln/
Ich nehme an du kennst die Antwort bereits. Chemie ist nicht mein Gebiet, deswegen möchte ich es auch nur streifen. Ich würde sagen, wenn es für Atome energetisch günstiger ist eine Verbindung mit anderen Atomen einzugehen, anstatt als einzelnes Teilchen zu sein, dann ja wird bei der Verbindung wohl diejenige Energie frei, die sie dadurch einsparen.Gim schrieb:Wird grundsätzlich Energie frei, wenn sich Atome zu Molekülen zusammenlagern? Oder nur in bestimmten Konstellationen?
hm hast wohl recht, Hydrogen Isotope zerfallen..jedoch "The proton has never been observed to decay and hydrogen-1 is therefore considered a stable isotope. Some recent theories of particle physics predict that proton decay can occur with a half-life of the order of 10^36 years. If this prediction is found to be true, then hydrogen-1 (and indeed all nuclei now believed to be stable) are only observationally stable. To date however, experiments have shown that if proton decay occurs, the half-life must be greater than 6.6 × 1033 years."Gim schrieb:Wenn überhaupt sind es 10^31 Jahre, nicht 1031. Bitte nicht so plump kopieren. Davon allerdings abgesehen ist der Protonenzerfall keineswegs nachgewiesen. Die Behauptung, dass alle Atome zerfallen ist damit nicht stichhaltig.
Bei Dingen, die sich unterscheiden wählt man als, bei Dingen die gleich sind wie. Kleiner, größer, besser, schlechter dümmer, klüger als jemand oder etwas anderes, aber genauso wie etwas anders. Inhaltlich war die Aussage ebenfalls nicht geglückt. Weder sind U-235 und U-238 stabil, noch ist U-236 wesentlich instabiler als U-235.
unglücklich formuliert, aber bei aller Kritik, nicht falsch, ich schrieb
Uran-235 ist weniger stabil wie Uran-238......wenn man es in Ruhe lässt beträgt seine Halbwertzeit 7,1 x 108 Jahre"stabil" ist hier Zerfallsrate gemeint (und beim Kopieren ging das Hochzeichnen verloren.)
Uran-235 ---> 7,1 x 10^8 Jahre
Uran 238 ---> 4,5 * 10^9 Jahre
Der erste Satz ist sehr schlecht gewählt, U-236 hat eine sehr hohe Halbwertszeit, hier ist "instabil" im Zusammenhang des Einfanges des Neutrons gemeint und dem Auseinanderbrechen, was im zweiten Satz dann auch hervorgeht.Gim schrieb:Davon abgesehen ist neutroneninduzierte Kernspaltung nicht mit radioaktivem Zerfall gleichzusetzen, auch wenn beides themenverwandt ist.
und was "induzierte Kernspaltung ist", siehe z.B. hiermayday schrieb:Uran-236 ist ein sehr instabiles Isotop und zerfällt rasch in leichtere Atome und Teilchen. Diesen Vorgang nennt man "induzierte Kernspaltung"
http://www.gutefrage.net/frage/induzierte-kernspaltung-von-uran (Archiv-Version vom 18.06.2016)
Du hast ja recht, aber das hier ist keine wissenschaftliche Arbeit und auch was du schreibst hat mängel, denn Brennstäbe können auch z.B. im Abklingbecken schmelzen, dann wenn das Wasser verdampft und und alle auf einem Haufen liegt z.B. weil das Gebäude einstürzt. Gemeint war, dass im einem AKW die Kettenreaktionsrate von Menschen erhöht oder gedrosselt wird, wir es kontrollieren...bei einer Kernschmelze ist es uns entglitten und brutzelt vor sich hin.Gim schrieb:Eine Kernschmelze ist das Schmelzen eines Reaktorkerns. Ohne einen Kernreaktor kann also keine Kernschmelze stattfinden. Eine unkontrollierte Kettenreaktion ist also keine Kernschmelze.
korrektGim schrieb:Radium ist kein Gas sondern ein Erdalkalimetall.
mayday schrieb:In dieser Decayfolge ist auch Polinium-216 zu finden.
korrektGim schrieb:Das deutsche Wort ist Zerfallsreihe.